Autor:
Lewis Jackson
Data Creației:
5 Mai 2021
Data Actualizării:
1 Iulie 2024

Conţinut
Mol este unitatea standard de măsură în chimie, utilizată pentru a analiza diferitele elemente dintr-un compus. De obicei, masa compusă este calculată în grame (g) și trebuie convertită în unități molare. Tranziția este destul de simplă, cu toate acestea, există încă câțiva pași importanți pe care trebuie să-i urmăm. Folosind metoda de mai jos, puteți converti cu ușurință grame în alunițe.
Pași
Partea 1 din 2: Calculați masa moleculară
Pregătiți consumabilele necesare pentru a rezolva problema matematicii. Când aveți toate instrumentele disponibile, va fi mai ușor să rezolvați problema. Ceea ce aveți nevoie este:
- Creion și hârtie. Matematica devine mai ușoară atunci când scrieți totul pe hârtie. Trebuie să parcurgi toți pașii pentru a obține un scor maxim.
- Tabel periodic al elementelor chimice: utilizat pentru determinarea atomilor de masă ai elementelor.
- Calculator de buzunar: folosit pentru a calcula numere complicate.

Determinați ce elemente sunt în compusul pe care trebuie să îl convertiți în unități molare. Primul pas în calcularea masei moleculare este determinarea elementelor care alcătuiesc compusul. Acest lucru este ușor, deoarece abrevierea pentru elemente este de numai unul sau două caractere.- Dacă o substanță este prescurtată cu două caractere, prima literă este scrisă cu majusculă, iar a doua literă este minusculă. Exemplu: Mg este abrevierea pentru elementul magneziu.
- Compuși NaHCO3 este format din patru elemente: sodiu (Na), hidrogen (H), carbon (C) și oxigen (O).
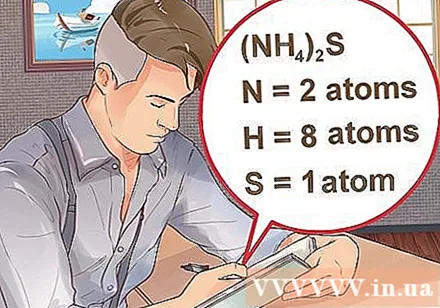
Determinați numărul de atomi pentru fiecare element din compus. Trebuie să cunoașteți numărul atomic al fiecărei substanțe dintr-un compus pentru a calcula molecula de masă a acelui compus. Numărul mic de lângă abrevierea elementului reprezintă numărul atomic al elementului.- Exemplu: compusul H2O are doi atomi de hidrogen și un atom de oxigen.
- Dacă un compus este scris între paranteze, urmat de un indice mic, fiecare ingredient dintre paranteze înmulțește indicele. Exemplu: compus (NH4)2S este format din doi atomi de N, opt atomi de H și un atom de S.

Notați hârtia atomică cubică pentru fiecare element. Utilizarea tabelului periodic este cel mai simplu mod de a găsi atomul cub al unui element. După ce localizați elementul pe tabelul periodic, veți vedea masa atomică chiar sub pictograma elementului.- De exemplu, atomul cub de oxigen este 15,99.
Calculați masa moleculară. Molecula de masă a unei substanțe este egală cu numărul de atomi ai fiecărui element înmulțit cu atomul de masă al acelui element. Această cantitate este esențială în conversia gram în molar.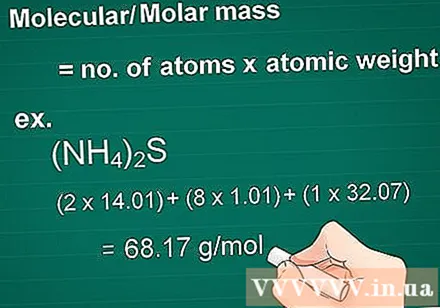
- În primul rând, înmulțiți numărul atomic al fiecărui element din compus cu atomul său de masă.
- Apoi, adăugați împreună masele elementelor din compus.
- Exemplu: Masa moleculară a unui compus (NH4)2S = (2 x 14,01) + (8 x 1,01) + (1 x 32,07) = 68,17 g / mol.
- Masa moleculară este, de asemenea, cunoscută sub numele de masă molară.
Partea 2 din 2: Convertiți grame în mol
Configurați formula de conversie. Pentru a găsi numărul de moli al compusului, împărțiți numărul de grame al compusului la masa molară a acelui compus.
- Formula: numărul de moli = masa (grame) / masa molară a compusului (gram / mol)
Înlocuiți numerele în formulă. După configurarea formulei corecte, următorul pas este înlocuirea numerelor pe care le-ați calculat în formulă. Dacă doriți să vă asigurați că datele sunt în poziția corectă, le puteți verifica suprimând unitatea. Dacă după simplitate unitatea rămasă este alunițe, atunci sunteți setat corect.
Rezolvați ecuația. Folosind un calculator, împărțiți masa la molecula cubică a substanței sau a compusului. Coeficientul va fi numărul de moli de substanță sau compus pe care îl căutați.
- De exemplu, problema este pentru 2 g de apă (H2O) și vă cer să o convertiți în unități molare. Avem masa molară a lui H2O este 18g / mol. Împarte 2 la 18, astfel încât să ai 0,1111 mol H2O.
Sfat
- Nu uitați să includeți elementul sau numele compusului cu răspunsurile.
- Dacă vi se cere să prezentați exercițiul sau testul, asigurați-vă că vă arătați clar răspunsurile, încercuind sau desenând o cutie în jurul răspunsurilor.
De ce ai nevoie
- Tabel periodic chimic
- Creion
- Hârtie
- Calculator
- Probleme de chimie



