Autor:
Bobbie Johnson
Data Creației:
10 Aprilie 2021
Data Actualizării:
1 Iulie 2024

Conţinut
- Pași
- Partea 1 din 2: Pregătiți echipamentul
- Partea 2 din 2: Realizați un experiment
- sfaturi
- Avertizări
- De ce ai nevoie
Procesul de scindare a apei (H2O) în constituenții săi (hidrogen și oxigen) folosind electricitate se numește electroliză. Gazele obținute ca urmare a electrolizei pot fi folosite singure - de exemplu, hidrogenul servește ca una dintre cele mai curate surse de energie. Deși numele acestui proces poate părea puțin inteligent, este de fapt mai ușor decât s-ar părea dacă aveți echipamentul potrivit, cunoștințele și puțină experiență.
Pași
Partea 1 din 2: Pregătiți echipamentul
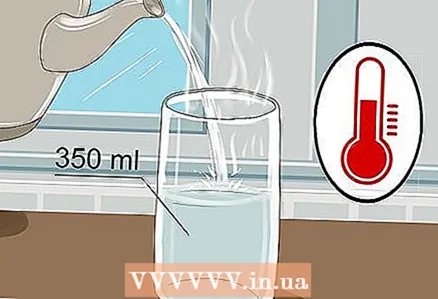 1 Luați un pahar de 350 ml și turnați apă caldă în el. Nu este nevoie să umpleți paharul până la refuz, este suficientă doar puțină apă. Apa rece va funcționa, deși apa caldă conduce electricitatea mai bine.
1 Luați un pahar de 350 ml și turnați apă caldă în el. Nu este nevoie să umpleți paharul până la refuz, este suficientă doar puțină apă. Apa rece va funcționa, deși apa caldă conduce electricitatea mai bine. - Atât apa de la robinet, cât și apa îmbuteliată vor funcționa.
- Apa caldă are o vâscozitate mai mică, ceea ce facilitează mișcarea ionilor.
 2 Se dizolvă 1 lingură (20 grame) de sare de masă în apă. Se toarnă sare într-un pahar și se amestecă apa pentru a se dizolva. Aceasta va crea o soluție salină.
2 Se dizolvă 1 lingură (20 grame) de sare de masă în apă. Se toarnă sare într-un pahar și se amestecă apa pentru a se dizolva. Aceasta va crea o soluție salină. - Clorura de sodiu (adică sarea de masă) este un electrolit care crește conductivitatea electrică a apei. În sine, apa nu conduce electricitatea bine.
- După ce creșteți conductivitatea electrică a apei, curentul creat de baterie va trece mai ușor prin soluție și va descompune mai eficient moleculele în hidrogen și oxigen.
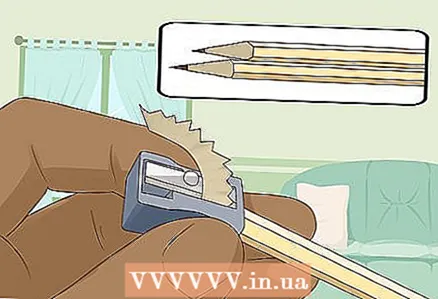 3 Ascuți două creioane dure și moi la ambele capete pentru a expune plumbul. Nu uitați să scoateți guma din creioane. O tijă de grafit ar trebui să iasă la ambele capete.
3 Ascuți două creioane dure și moi la ambele capete pentru a expune plumbul. Nu uitați să scoateți guma din creioane. O tijă de grafit ar trebui să iasă la ambele capete. - Tijele din grafit vor servi drept electrozi izolați la care conectați bateria.
- Grafitul este potrivit pentru acest experiment, deoarece nu se dizolvă și nu se corodează în apă.
 4 Tăiați o foaie de carton suficient de mare pentru a se așeza deasupra paharului. Folosiți o bucată de carton destul de groasă, care nu se va lăsa după ce ați perforat două găuri în ea. Tăiați o bucată pătrată dintr-o cutie de pantofi sau similar.
4 Tăiați o foaie de carton suficient de mare pentru a se așeza deasupra paharului. Folosiți o bucată de carton destul de groasă, care nu se va lăsa după ce ați perforat două găuri în ea. Tăiați o bucată pătrată dintr-o cutie de pantofi sau similar. - Cartonul este folosit pentru a ține creioanele în apă, astfel încât să nu atingă părțile laterale și fundul paharului.
- Cartonul nu este conductiv, deci îl puteți pune în siguranță pe un pahar.
 5 Folosiți creioane pentru a introduce două găuri în carton. Înțepați cartonul cu creioane - în acest caz, acestea vor fi strânse bine și nu vor aluneca. Asigurați-vă că grafitul nu atinge părțile laterale sau fundul sticlei, altfel va interfera cu experimentul.
5 Folosiți creioane pentru a introduce două găuri în carton. Înțepați cartonul cu creioane - în acest caz, acestea vor fi strânse bine și nu vor aluneca. Asigurați-vă că grafitul nu atinge părțile laterale sau fundul sticlei, altfel va interfera cu experimentul.
Partea 2 din 2: Realizați un experiment
 1 Conectați un fir cu cleme de aligator la fiecare terminal al bateriei. Bateria va servi ca sursă de curent electric, iar prin firele cu cleme și tije de grafit, curentul va ajunge în apă.Conectați un fir cu o clemă la pozitiv și celălalt la borna negativă a bateriei.
1 Conectați un fir cu cleme de aligator la fiecare terminal al bateriei. Bateria va servi ca sursă de curent electric, iar prin firele cu cleme și tije de grafit, curentul va ajunge în apă.Conectați un fir cu o clemă la pozitiv și celălalt la borna negativă a bateriei. - Folosiți o baterie de 6 volți. Dacă nu aveți una, puteți folosi în schimb o baterie de 9 volți.
- O baterie adecvată poate fi obținută de la un magazin de alimentare cu energie electrică sau supermarket.
 2 Conectați celelalte capete ale firelor la creioane. Atașați ferm clemele de sârmă metalică la tijele de grafit. Este posibil să trebuiască să mai scoateți din lemn creioane pentru a împiedica alunecarea clemelor de pe tijele de grafit.
2 Conectați celelalte capete ale firelor la creioane. Atașați ferm clemele de sârmă metalică la tijele de grafit. Este posibil să trebuiască să mai scoateți din lemn creioane pentru a împiedica alunecarea clemelor de pe tijele de grafit. - Astfel, veți închide circuitul, iar curentul din baterie va curge prin apă.
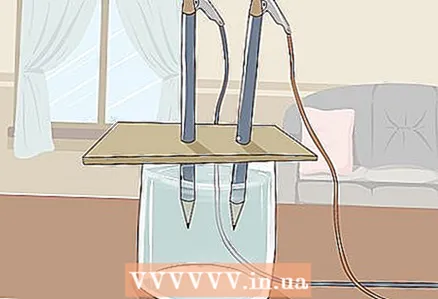 3 Așezați cartonul pe sticlă, astfel încât capetele libere ale creioanelor să fie scufundate în apă. Foaia de carton ar trebui să fie suficient de mare pentru a sta pe sticlă. Aveți grijă să nu deranjați așezarea corectă a creioanelor.
3 Așezați cartonul pe sticlă, astfel încât capetele libere ale creioanelor să fie scufundate în apă. Foaia de carton ar trebui să fie suficient de mare pentru a sta pe sticlă. Aveți grijă să nu deranjați așezarea corectă a creioanelor. - Pentru ca experimentul să aibă succes, grafitul nu trebuie să atingă pereții și fundul sticlei. Verificați din nou acest lucru și reglați creioanele, dacă este necesar.
 4 Urmăriți cum apa se împarte în hidrogen și oxigen. Bulele de gaz vor începe să crească din tijele de grafit cufundate în apă. Acestea sunt hidrogen și oxigen. Hidrogenul va fi eliberat la polul negativ și oxigenul la polul pozitiv.
4 Urmăriți cum apa se împarte în hidrogen și oxigen. Bulele de gaz vor începe să crească din tijele de grafit cufundate în apă. Acestea sunt hidrogen și oxigen. Hidrogenul va fi eliberat la polul negativ și oxigenul la polul pozitiv. - De îndată ce conectați firele la baterie și tijele de grafit, un curent electric va curge prin apă.
- Pe creionul care este conectat la polul negativ se vor forma mai multe bule de gaz, deoarece fiecare moleculă de apă este formată din doi atomi de hidrogen și un atom de oxigen.
sfaturi
- Dacă nu aveți creioane cu arbori de grafit, puteți folosi în schimb două fire mici. Înfășurați doar un capăt al fiecărui fir în jurul stâlpului corespunzător al bateriei și înmuiați-l pe celălalt în apă. Rezultatul va fi același ca la creioane.
- Încercați să utilizați o baterie diferită. Cantitatea de curent care curge depinde de tensiunea bateriei, care, la rândul său, afectează rata de divizare a moleculelor de apă.
Avertizări
- Dacă adăugați un electrolit, cum ar fi sare, în apă, rețineți că experimentul va genera o cantitate mică dintr-un produs secundar, cum ar fi clorul. Este sigur în cantități atât de mici, dar puteți simți un miros ușor de clor.
- Efectuați acest experiment sub supravegherea unui adult. Este asociat cu electricitatea și gazele și, prin urmare, poate fi periculos, deși puțin probabil.
De ce ai nevoie
- Două creioane dure și moi
- O baterie de 6 sau 9 volți
- Sticlă cu un volum de 350 mililitri
- 2 fire cu cleme de crocodil
- Ascuțitor pentru creion
- Sare



